Proč je vodík pro vědce i politiky zajímavý a jak si stojí mezi ostatními alternativními palivy, jste se dozvěděli v tomto článku. Vodík jako palivo budoucnosti se již nyní používá i v městské hromadné dopravě nebo třeba pro napájení mobilních telefonů. Více zde..
Nyní přinášíme tento více technicky založený článek se záměrem osvětlit všechny klíčové technologické celky vodíkového hospodářství. Logicky začneme od výroby vodíku přes možnosti jeho skladování až po palivové články a nastíníme si také otázku bezpečnosti související s využíváním vodíku.
Výroba vodíku
Vodík může být vyráběn mnoha způsoby z širokého spektra vstupních zdrojů. Roční světová produkce vodíku je přibližně 55 milionů tun. V globálním měřítku dominuje v současné době výroba z fosilních paliv.
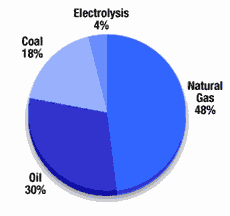
Zastoupení různých způsobů výroby vodíku ve světovém měřítku
Využívání takto vyrobeného vodíku může pomoci lokálně snížit produkci některých zdraví poškozujících látek, globálně by však vedlo pouze k méně hospodárnému využívaní primární energie a s tím souvisejícímu nárůstu produkce oxidu uhličitého (a dalších škodlivých látek). Další možností je výroba vodíku z obnovitelných zdrojů. S jejich využitím se vodík získává pomocí elektrolýzy vody, vysokoteplotního rozkladu vody, zplyňováním či pyrolýzou biomasy nebo výrobou s využitím speciálních bakterií.
Pro výrobu vodíku přímo z vody se jeví vhodné také některé vyvíjené jaderné reaktory čtvrté generace. Vysoká teplota chladiva na výstupu z reaktoru je ideální pro některé perspektivní termochemické cykly i vysokoteplotní elektrolýzu.
Hlavním motorem rozvoje vodíkového hospodářství je nalezení alternativy k využívání fosilních paliv, a to především v dopravním sektoru. Případná masivní výroba vodíku pro tyto účely z fosilních paliv by proto byla z výše uvedených důvodů jen těžko obhajitelná, a proto se pozornost v poslední době soustředí na ty způsoby výroby vodíku, které neprodukují emise škodlivých látek a nejsou závislé na dodávkách fosilních paliv.
Stručný přehled výrobních technologií vodíku:
Jak již bylo řečeno, možností jak vodík vyrábět existuje celá řada, přičemž v dalším textu se zaměříme na nejrozšířenější, případně v současné době nejperspektivnější technologie výroby vodíku.
Parní reforming zemního plynu
Tato technologie je v současnosti nejlevnějším a nejrozšířenějším způsobem výroby vodíku. Teplo pro reformní reakci i následnou konverzi oxidu uhelnatého je dodáváno z přímého spalování části zemního plynu (tzv. autotermní reforming).
Proces má dvě fáze; v první se za přítomnosti katalyzátoru do vodní páry (500 - 1 100o C, 0,3 - 2,5 MPa) přivádí metan (dominantní část zemního plynu). Směs metanu a páry reaguje za vzniku vodíku a oxidu uhelnatého a menšího podílu oxidu uhličitého. Poté následuje navyšování množství produkovaného vodíku konverzí CO z reforméru s další přidanou párou. Reakce probíhá již za nižších teplot.
reformní reakce: CH4 + H2O → CO + 3H2
konverze CO: CO + H2O → CO2 + H2
Účinnost (konverze) produkce vodíku je závislá na poměru páry a uhlíku ve směsi; pohybuje se okolo 80 %. Značnou nevýhodou je produkce vysokého množství oxidu uhličitého - na 1 kg vodíku se vyprodukuje 7,05 kg CO2.
Elektrolýza vody
Elektrolýza vody je proces, při kterém stejnosměrný proud při průchodu vodou (většinou s přídavkem dalších látek pro zvýšení vodivosti) rozštěpí chemickou vazbu mezi vodíkem a kyslíkem:
2H2O → 2H2 + O2
H+ (proton) poté reaguje na katodě za vzniku plynu, který je jímán a následně skladován. Proces elektrolýzy probíhá za pokojových teplot a pro jeho chod je nutná pouze elektrická energie. Tímto způsobem jsou vyrobena asi 4 % z celkové světové produkce vodíku, který je využíván zejména tam, kde je třeba vysoce čistý vodík.
Účinnost procesu se pohybuje v rozmezí 80 - 92 %. Výstupem elektrolýzy je kyslík a vysoce čistý vodíkový plyn, pro většinu aplikací bez nutnosti dodatečného dočišťování. Na celkové účinnosti elektrolytické výroby vodíku se podílí především účinnost výroby elektrické energie (30 - 40 % pro konvenční zdroje). Celková účinnost elektrolýzy se tedy pohybuje přibližně v rozmezí 25 - 35 %. Výhodu je současná produkce kyslíku, který má podobně jako vodík široké využití.
Pro lepší představu: osobní vodíková vozidla mají spotřebu okolo 1kg vodíku na 100 km. Na výrobu tohoto množství vodíku elektrolýzou je třeba přibližně 9kg (~9 litrů) vody a 60kWhel.
Vysokoteplotní elektrolýza
Pro vysokoteplotní elektrolýzu, nazývanou též někdy parní elektrolýza, je charakteristické, že část dodávané energie tvoří elektrická energie a část je přivedena ve formě tepla, čímž je zvýšena celková účinnost procesu oproti klasické elektrolýze vody. Reakce probíhající ve vysokoteplotním elektrolyzéru je reverzní k reakci probíhající v palivových článcích s pevnými oxidy. Do elektrolyzéru vstupuje vodní pára a vodík; vystupuje z něho obohacená směs obsahující 75 % hm vodíku a 25 % hm páry. Vodík je pak z páry oddělen v kondenzační jednotce. Celková účinnost vysokoteplotní elektrolýzy (vč. výroby potřebné energie) může dosahovat až 45 %. Tato metoda je vedle termochemických cyklů štěpení vody, popsaných v dalším odstavci, slibným kandidátem na výrobu vodíku ve velkém měřítku.
Termochemické cykly štěpení vody
Termochemické cykly jsou známy již více jak 35 let; intenzivně byly studovány na přelomu 70. a 80. let 20. století (v době ropné krize, tedy v době hledání ekonomické výroby alternativních paliv). Při termochemickém štěpení vody je voda rozdělena na kyslík a vodík pomocí série chemických reakcí, které využívají energie ve formě vysokopotenciálního teple anebo v případě hybridních cyklů tepla a elektřiny. Cykly popisované níže jsou cykly uzavřené, tj. použité chemické látky jsou v průběhu reakcí "recyklovány" a znovu vstupují do procesu. Doplňovanou vstupní surovinou je tedy pouze voda a výsledným produktem vodík a kyslík.
S-I cyklus
Siřičito-jódový termochemický cyklus byl vyvinut v General Atomics (San Diego, USA) v polovině 70. let 20. století. Je předním kandidátem levné a účinné výroby vodíku pomocí jaderné energie.
Vstupní surovinou je pouze voda a vysokopotenciální (s vysokou teplotou média) teplo; výstupními surovinami jsou kyslík s vodíkem a nízkopotenciální teplo. Všechny vstupní suroviny jsou tekuté. Jód a oxid siřičitý se recyklují a opětně používají, teoreticky se tedy neprodukuje žádný odpad (ve skutečnosti samozřejmě k určitým ztrátám dochází). Při produkci vodíku probíhají tyto termochemické reakce:
I2 + SO2 + 2H2O → 2HI + H2SO4 (120o C)
H2SO4 → SO2 + H2O + 1/2O2 (800-1 000o C)
2HI → I2 + H2 (300-450o C)
V prvním kroku, který je znám jako Bunsenova reakce, reaguje vstupující voda s jódem a oxidem siřičitým za vzniku kyseliny sírové a jodovodíkové. Nejvíce tepla (a o nejvyšší teplotě, 800-1000 oC) vyžaduje endotermický rozklad kyseliny sírové. Rozklad kyseliny jodovodíkové a současná produkce vodíku vyžaduje teploty nižší (450o C).
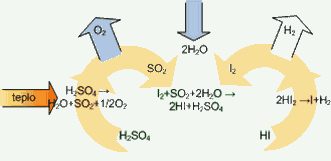
Schéma SI procesu štěpení vody
Účinnost celého výrobního cyklu vodíku se pohybuje v rozmezí 40-52 % (50 % při 950o C ). S dalším nárůstem teplot bude růst i účinnost cyklu. Oproti elektrolýze má vyšší účinnost, protože není třeba vyrobené teplo přeměňovat se ztrátami na elektřinu.
Nevýhodou tohoto cyklu je požadavek vysokých vstupních teplot a agresivita kyseliny sírové a jodovodíkové, což vede k vysokým nárokům na chemickou odolnost použitých materiálů. Problematická bude kontrola podmínek reakcí v průmyslovém měřítku (v laboratorních podmínkách byla tato otázka již zvládnuta). Podrobnosti k S-I cyklu i k dalším termochemickým cyklům můžete nalézt např. zde. (hytep.cz)

Laboratorní výroba H2 SI procesem v Japan Atomic Energy Research Institute (JAERI)
Mimo uvedené možnosti existuje celá řada dalších způsobů výroby vodíku, přičemž preference toho kterého způsobu vyplyne z lokálních dostupnosti surovin a energií, poptávky a především z investičních a provozních nákladů více než z celkové účinnosti procesu. Pro masivní udržitelnou výrobu se jeví perspektivní výroba vodíku chemickými cykly nebo vysokoteplotní elektrolýza v kombinaci s vysokopotencionálním zdrojem tepla - vybrané reaktory tzv. Generace IV.
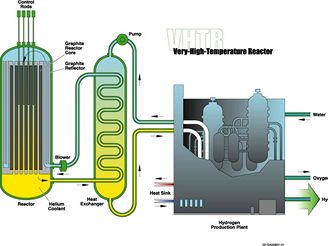
Vysokoteplotní reaktor IV. Generace, chlazený He, moderovaný grafitem
Konvenční elektrolýza najde pravděpodobně uplatnění v menších lokálních zdrojích vodíku. Elektrická energie z obnovitelných zdrojů může být s výhodou využita právě pro lokální výrobu vodíku, odstraňuje komplikace s regulací energetické přenosové soustavy. Bioplyn a ostatní obnovitelná biologická paliva bude pravděpodobně výhodnější spalovat přímo ve spalovacích motorech či v menších zdrojích elektrické energie. Výroba vodíku se také může stát perspektivní metodou regulace spotřeby elektrické energie.
Biotechnologická produkce vodíku
Jiným zajímavým způsobem, který je dnes ovšem na počátku vývoje, je výroba vodíku pomocí mikroorganismů.
Ačkoli "suchá" biomasa je vhodným materiálem pro konverzi pomocí klasických termochemických procesů, biomasa s vysokým obsahem vody je tímto způsobem z ekonomického hlediska nevyužitelná. Proto může být v případě vlhké biomasy výhodné využít biotechnologické procesy, kdy reakce jsou katalyzovány mikroorganismy ve vodném prostředí za nízkých teplot a tlaků. V tomto případě rozlišujeme dva procesy: vodíkovou fermentaci (i) fungující bez přítomnosti světla a fotobiologickou produkci vodíku (ii).
Vodíková fermentace v nepřítomnosti světla je přirozený děj ke kterému dochází za anoxických nebo anaerobních podmínek. Organické látky jsou v tomto případě využívány jako primární zdroj vodíku a také jako zdroj energie. Různé druhy bakterií využívají v nepřítomnosti kyslíku redukci protonů na vodík k uložení elektronů z oxidace organických látek. Pro plné využití chemické energie substrátu jsou potřeba dva kroky, jak je ukázáno na Obr. 1. V první fázi je z organického substrátu produkován vodík pomocí vodíkové fermentace. V druhé fázi je pak z efluentu obsahujícího acetát získáván buďto bioplyn nebo pomocí fotofermentace (viz níže) vodík. Dále je vhodné využít biologicky nerozložitelné zbytky biomasy, které je obvykle možno spalovat. Tím se dosáhne dalšího zvětšení množství získané energie.
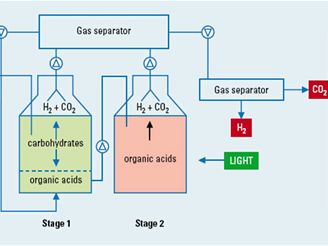
Schéma bioprodukce vodíku pomocí dvoustupňové fermentace
Fotofermentace je proces, při kterém jsou organické látky, například acetát, bakteriemi přeměňovány na vodík a CO2 za využití světla. Proces probíhá za anaerobních podmínek a může být snadno kombinován s vodíkovou fermentací popsanou výše, kde je acetát jedním z produktů. Jednou ze skupin mikroorganismů schopných fotofermentace jsou purpurové bakterie. Ačkoli bylo do dnešní doby navrženo mnoho fotobioreaktorů, v praxi nalezl dosud uplatnění pouze typ uvedený na (Obr. 2).
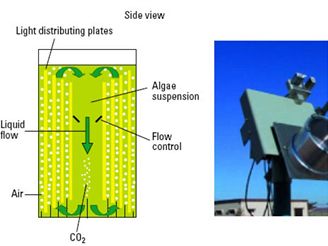
Design "flat-plate" fotobioreaktoru; prototyp slunečního kolektoru
Výroba vodíku pomocí mikroorganismů je slibným, nicméně v celkovém pohledu poněkud nízkokapacitním způsobem jak vodík vyrábět. Velkou výhodou oproti např. výrobě uhlovodíkových biopaliv je využití vstupních surovin, které jsou jinak obtížně zpracovatelné (např. kaly z čističek odpadních vod), a nekonkuruje tak z hlediska záborů orné půdy výrobě potravin.
|
Porovnání celkových účinností jednotlivých koncepcí zde a zde. |
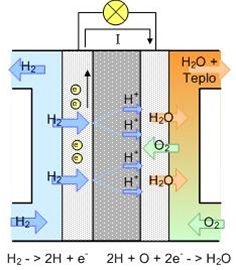
Palivové články
Palivový článek je zařízení, které při elektrochemické reakci přeměňuje chemickou energii kontinuálně přiváděného paliva s oxidačním činidlem na energii elektrickou.
Oproti tepelným strojům s generátorem el. energie dosahují palivové články při výrobě elektrické energie vysokých účinností, a to až 60 % v laboratorních podmínkách. Reálná účinnost dosahuje 40-55 %, dle zatížení a typu palivového článku. Vysoká účinnost je dána zejména tím, že přeměna energie je přímá, nikoliv přes mezistupně (tepelnou a mechanickou E), jako je tomu např. u spalovacích motorů.
V současné době je vyvíjeno pět typů palivových článků lišících se především chemickým složením elektrolytu, provozními teplotami a možným palivem. Nízkoteplotní palivové články využívají s kyslíkem (většinou ze vzduchu) vodík nebo methanol, vysokoteplotní články mohou využívat i některá konvenční uhlovodíková paliva. Jednotlivé typy článků vhledem k rozdílným provozním parametrům nacházejí uplatnění ve velmi odlišných aplikacích. Nízkoteplotní palivové články jsou využívány zejména v mobilních aplikacích k výrobě elektrické energie, vysokoteplotní články naopak převládají v kombinované výrobě tepla a elektrické energie v aplikacích stacionárních.
Soubor dvou elektrod a elektrolytu je nazýván palivovou celou, palivovým článkem obvykle označujeme soubor palivových cel. (analogie s chemickými bateriemi). Palivové články jsou obvykle sestaveny z palivových cel v bipolárním uspořádání s ohledem na požadované výstupní parametry článku (především napětí a výkon).
Princip palivového článku lze nejsnáze objasnit na palivovém článku s polymerní membránou. Tento článek se skládá ze dvou elektrod, na jejichž povrchu se nachází slabá vrstvička uhlíku (většinou ve formě grafitu) obsahujícím malé množství platiny, která zde slouží jako katalyzátor.

Grafit s rozptýlenými částečkami platiny (tmavé tečky)
Elektrody jsou od sebe odděleny tenkou polymerní membránou, která propouští kladně nabité ionty - protony (u katexové membrány). Vodík je přiváděn k anodě, kde na povrchu katalyzátoru dochází k jeho disociaci na protony a elektrony. Protony procházejí skrze polymerní vrstvu, elektrony jsou nuceny procházet externím okruhem, a mohou tedy konat užitečnou práci. Na katodě pak sloučením dvou kladně nabitých vodíkových iontů (protonů), dvou elektronů a atomu kyslíku vzniká voda (vzhledem k provozní teplotě palivového článku obvykle v podobě páry). Na stranu katody je přiváděn čistý kyslík nebo častěji kyslík ze vzduchu.
Ostatní typy palivových článků jsou stručně popsány např. zde (hytep.cz).

Příklad palivového článku složeného z 30 cel
Palivové články jsou v současnosti technologicky velmi vyspělá a bezpečná zařízení. Jejich komerčnímu rozšíření braní prozatím jejich vysoká cena daná stupněm vývoje a převážně kusovou výrobou a v neposlední řadě cenou použitých materiálů. U nízkoteplotních palivových článků je to především cena fluorovaných membrán a platiny, u vysokoteplotních potom cena materiálů schopných odolat vysokým teplotám a korozivnímu prostředí. Cena palivového PEM článku je v současnosti přibližně 3 000-4 000 USD/kW. Přední výrobci však již dnes garantují budoucí cenu/kW srovnatelnou se špičkovým spalovacím motorem.
Skladování vodíku
Možnost dlouhodobého skladování vodíku představuje základní technologickou výhodu oproti dalšímu nosiči energie – elektřině, u které je nutno neustále regulovat rovnováhu mezi výrobou a spotřebou. "Uskladnění" elektřiny v akumulátorech není využitelné v měřítku velkovýroby, přečerpávací elektrárny jsou sice užitečnou, ale opět poněkud okrajovou možností. Skladování vodíku tedy představuje velmi výhodnou možnost, jak optimalizovat a regulovat výrobu a spotřebu energií obecně. Existují například plány na propojené výroby elektřiny a vodíku přes elektrolýzu, což by umožnilo snazší regulaci jaderných elektráren, které by mohly pracovat při optimálním zatížení po celou dobu a v období sníženého odběru by se vyráběl vodík, využitelný buď pro výrobu elektřiny (v době špičky) nebo pro dopravu. Popsané propojení by bylo užitečné i u jiných typů elektráren, viz problémy s regulací energetické soustavy SRN v loňském roce z důvodu nadvýroby elektřiny z větrných elektráren. Nicméně některé fyzikálně-chemické vlastnosti vodíku nám jeho uskladňování trochu komplikují, jako např. jeho velmi nízká hustota a bod varu.
Skladování vodíku v plynné fázi
Pro stacionární aplikace se obvykle používá ocelových bezešvých lahví z nízkouhlíkaté nebo legované oceli. Vyrábějí se v objemech od 0,8 litrů až do přibližně 140 l pro běžné aplikace.V mobilních aplikacích se obvykle používá kompozitních tlakových nádob. Vyrábějí se v objemech od desítek litrů až přibližně do 300 l. Typickým provozním tlakem je 350 bar (=350 atm = 35MPa), v nejnovějších aplikacích potom 450 až 700 bar (současný technologický limit je 1 000 bar). V mnoha aplikacích je válcový tvar mírně deformován v závislosti na potřebách zástavby do úložného prostoru vozidla. Vnitřní povrch kompozitních lahví tvoří obvykle tenká vrstva kovu, případně speciálního polymeru, která zabraňuje úniku plynu přes strukturu kompozitu.

Průřez kompozitní lahví pro plynný H2
Pokud chceme skladovat vodík ve vysokotlakých nádržích, musíme jej nejprve stlačit na požadovaný tlak. Pro stlačování vodíku se používá zejména pístových kompresorů. Energie potřebná na stlačení vodíku na 350 bar dosahuje přibližně 30 % energie v palivu.
Skladování vodíku v kapalné fázi:
Běžně využívaná fosilní paliva je možné skladovat v kapalném stavu za běžných teplot a při relativně nízkých tlacích, oproti tomu kapalný vodík je skladován při teplotě -252 şC; s tím souvisejí zvýšené nároky na použité materiály a vysoké energetické nároky na zkapalnění.

Průřez nádrží na kapalný vodík
Vodík je ze zásobníku čerpán jako kapalina - pro spalovací motory nebo jako plyn - pro palivové články. Pro uskladnění se používají vícevrstvé nádoby s velmi dobrými izolačními vlastnostmi s maximálním přetlakem 5 barů. Tyto nádoby musí být vybaveny přetlakovým mechanismem, kterým je regulován maximální přípustný tlak. Při skladování vodíku v kryogenních nádobách dochází vlivem přestupu tepla z okolí k postupnému odpařování, a tedy zvyšování tlaku uvnitř této nádoby. Aby nedošlo k destrukci nádrže, musí být tlak uvnitř nádoby regulován odpouštěním odpařeného vodíku. Pro běžně používané nádrže dosahují ztráty až 3 % hm na den. V některých aplikacích je takto unikající vodík jímán a stlačován do přídavných tlakových lahví.
Zkapalňování vodíku je technologicky i energeticky náročný proces. Energie potřebná ke zkapalnění dosahuje přibližně 40 % energie v palivu.
Vedle těchto tradičních způsobů skladování existuje ještě velké množství alternativních technologií skladování vodíku. Nejperspektivnější se jeví skladovat vodík vázaný v materiálech, jako jsou alanáty, metalhydridy, nanostruktury uhlíku a další, viz skladování vodíku na hytep.cz.
Bezpečnost
Na úvod je třeba předeslat, že všechna paliva jsou nějakým způsobem nebezpečná. S nadsázkou by se dalo říci, že to je právě ta vlastnost, pro kterou se využívají. Vysoká hustota energie, hořlavost a výbušnost jsou vlastnosti, které jsou společné všem druhům paliv. Skladování těchto látek v prostoru vozidla představuje riziko vznícení, případně výbuchu paliva vně spalovací komory tepelného motoru nebo palivového článku. Vodík není v tomto ohledu výjimkou, přesto je jeho chování v mnoha ohledech velmi odlišné od stávajících fosilních paliv.
Vodík tvoří spolu se vzduchem hořlavou a výbušnou směs v širokém rozsahu koncentrací (4-75 % objemu pro hořlavou směs a 19-59 % objemu pro výbušnou směs); při rychlé expanzi může dojít k samovznícení; vodík má velmi nízkou zápalnou energii, již velmi malý elektrostatický náboj (0,02 J) může iniciovat vzplanutí paliva, nízká viskozita a malá velikost vodíkové molekuly kladou zvýšené nároky na utěsnění palivové soustavy. Únik vodíku není možné rozpoznat lidskými smysly. Velmi nízká hustota plynu napomáhá rychlému rozptylu do okolí, a tedy rychlému snížení koncentrace pod zápalnou mez. Nebyly zjištěny toxické účinky na člověka, při hoření nevznikají toxické zplodiny; za denního světla není vodíkový plamen téměř viditelný.
Přestože většina výše uvedených parametrů je z hlediska bezpečnosti oproti běžným palivům méně příznivých, mnoho praktických zkoušek prokázalo menší destrukční účinky vzplanutí vodíkové nádrže na vozidlo i menší riziko pro posádku. Na následujícím obrázku je test úniku a následného vznícení vodíku vs. stejná situace s vozidlem na benzin.
Test úniku a vznícení vodíku z vozidla
Při destrukci nádrže stoupá vodík díky své nízké hustotě velmi rychle vzhůru a případný požár vzniká ve větší míře vně vozidla. K zvýšení bezpečnosti přispívá i menší množství paliva skladovaného ve vozidlech. Bezpečnost se dá dále zvýšit vhodným umístěním skladovací nádrže (u autobusu například na střechu vozidla).
Na závěr je třeba připomenout, že využívání vodíku není novinkou posledních let. Ve velkém množství je spotřebováván například v ropných rafinériích při výrobě benzinů nebo v potravinářství při ztužování tuků. Relativně nové je pouze jeho využívání jako energetického nosiče. Velké množství dopravních prostředků v rámci demonstračních projektů na celém světě (Cute, HyFleet:Cute, ...) denně prokazuje, že je vodík pro tyto účely dostatečně spolehlivé a bezpečné palivo.
Závěr
Cílem tohoto článku bylo přiblížit všechny podstatné aspekty vodíkového hospodářství po technické stránce. Výčet technologií palivových článků, způsobu výroby a skladování i bezpečnosti zcela jistě není úplný. Přesto si myslíme, že může sloužit jako základní vodítko pro orientaci v alternativních způsobech skladování energie a jejího využití např. v dopravě a ostatních energetických potřebách moderní společnosti.
Technologie související s využitím vodíku v dopravě a v energetice zaznamenaly velmi překotný rozvoj, zejména v posledních dvaceti letech. Zvýšila se jejich účinnost, bezpečnost a v neposlední řadě uživatelská přívětivost. V dalších letech se začneme setkávat s jednotlivými produkty vodíkových technologií čím dál tím častěji.
|
Autor Ing. Luděk Janík
je vedoucím oddělení vodíkových technologií - Ústav jaderného výzkumu Řež - a ředitelem České vodíkové technologické platformy. |