Šukrat Mitalipov z oregonské univerzity je za posledních let nejspíše na pozornost zvyklý. V Kazachstánu narozený vědec pracuje na klonování savců včetně člověka, a tak ho asi nepřekvapuje, když jeho práce vzbuzuje silné reakce i u těch, kteří biologii jinak mnoho pozornosti nevěnují. Je ovšem otázkou, zda byl připravený na vlnu pozornosti, kterou především v USA vyvolala nově vydaná práce jeho skupiny v časopise Nature.
O co vlastně šlo? Vědci během v podstatě běžné procedury umělého oplodnění u nově oplodněného vajíčka opravili po otci zděděnou špatnou verzi genu MYBPC3. Nositelé byť jediné vadné kopie tohoto genu mají vrozenou srdeční vadu, tzv. hypertrofickou kardiomyopatii, která je sice velmi vzácná (cca 0,2 % populace), ale může vést k náhlé smrti v mladém věku. Stojí třeba za některými případy řídkých, ale šokujících úmrtí mladých sportovců přímo na hřišti.
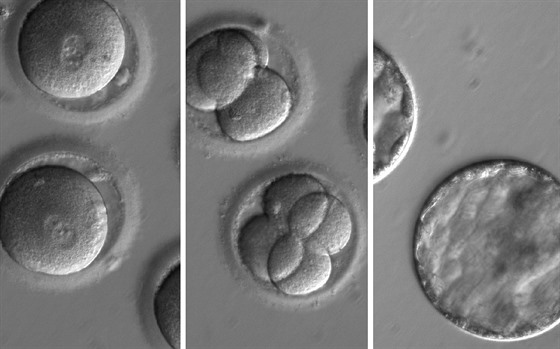
Špatnou verzi genu z DNA vajíčka vystřihli „nástrojem“ (spíše chemickým koktejlem) nazývaným CRISPR, aby ji hned vzápětí nahradili verzí správnou. Oplodněná vajíčka nechal tým tři dny vyvíjet, aby zjistil, jak si povedou, a pak byla zničena. Kdyby je hypoteticky nechal vyvíjet, zákrok by znamenal kompletní změnu DNA v celém organismu, protože k ní došlo hned na samém začátku vývoje jedince. Daný člověk by měl v těle výhradně opravené buňky.
Celá procedura je vlastně na pohled poměrně přímočará, jak se můžete přesvědčit na následujícím videu autorů. Je to samozřejmě klam, prakticky všechny práce před samotným vstříknutím chemikálií do vajíčka, ale nic to nemění na tom, že samotná manipulace je vlastně „nuda“:
Podobný kompletní přepis DNA je možný jen úplně na začátku vývoje organismu, protože zatím neznáme způsob, jak instrukce ke změně DNA dostat do všech buněk dospělého organismu. Genetické „editace“ u dětí či dospělých se tak provádějí na nějaké malé podmnožině buněk - například na buňkách imunitního systému.
Vajíčka s překvapením a další detailyByť vada, kterou autorský tým u k zániku odsouzených embryí „vyléčil“, může mít fatální následky, není to tak veliký medicínský problém, aby nutně vyžadoval zcela takto revoluční řešení. Volba na gen padla spíše proto, že jde o vzácný případ vady kódované jedním genem - a také zřejmě tím, že zrovna gen MYBPC3 se shodou okolností z DNA dobře „vystřihuje“. Jeden úspěch studie je v tom, že se téměř dokonale podařilo (s jednou výjimkou ze 112) zajistit, aby vyvíjející se embrya byla skutečně „opravená“. Editace se provedla v podstatě přímo během oplodnění - jedna dávka látek byla do kádinky s vajíčky vstříknuta současně se spermatem dárce. Přesto příroda v některých ohledech překvapila. Tým připravil vajíčkům v pokusu „náhradní díl“ - správný úsek DNA jako náhradu za vadný gen. Předchozí pokusy na dospělých buňkách ukázaly, že buňky po náhradním díle rády sáhnou. Ovšem všech 112 oplodněných vajíček v experimentu náhradu ignorovalo a raději si udělalo kopii správného genu z matčiny kopie DNA. Byť tedy pokus neproběhl úplně podle představ vědců, dopadl dobře. Úspěšnost postupu byla vysoká (těsně přes 70 procent embryí na konci neslo jen „zdravou“ DNA) a v embryích se také nepodařilo objevit velké vady. Neznamená to, že bychom mohli říci, že byla úplně bez následků a vyvinula by se zcela správně. Ani tak dobrý nástroj jako CRISPR není neomylný, dodejme, že podle některých kolegů autoři nezkontrolovali embrya tak podrobně, jak by asi bylo záhodno, viz například blog biologa Paula Knoepflera, a tak by se možná nějaké drobné chyby našly - a není vyloučeno, že by to byly chyby osudné. |
Důvody, proč se genetické opravy, či úpravy v praxi zkouší jen v malém, nejsou výhradně technického rázu. Kompletní přepis DNA ve všech buňkách s sebou přinášejí řadu problémů - tím zásadním je, že dotyčný by je předal i svým dětem. A to je příliš velké riziko. Zatím se jednoduše stále přesně neví, jaké následky by podobné „hrátky“ s DNA mohly mít v dospělosti.
Dnešní vědecký konsensus zjednodušeně řečeno je, že „nezděditelné“ úpravy lidské DNA jsou v pořádku a je možné je prakticky zkoušet a vyvíjet, dědičné ne - respektive je lze provádět pouze v rámci výzkumu a nechat geneticky upravená lidská embrya vyvíjet jen krátce.
Nechat je vyvinout dále by při dnešním stavu vědomostí a technologie je doslova zbytečné hazardování s lidskými životy. A proto Mitalipov a spol. od začátku měli v plánu nechat (a také nechali) embrya vyvíjet jen pár dní. Ostatně kontrolní komise na jejich ústavu by jim ani nic jiného nepovolili - a i o těch pár dní museli bojovat (ne všechny přitom přesvědčili, že to vůbec bylo nutné, ale o tom dále).
Byť se tedy na první pohled mohlo zdát, že práce otevřela vzrušující a zároveň děsivé možnosti vytváření „geneticky modifikovaných lidí“, není to pravda. GMO utopie (či dystopie, jak je komu libo) se tedy nijak zásadně nepřiblížila. A to ani symbolicky.
Pokusy s úpravou genetické informace už totiž v posledních letech proběhly i jinde, a to nejdříve v Číně. „Západ“ tedy tak trochu dohání náskok Asie. Mitalipov a spol. sice zveřejnili ve své práci celou řadu zajímavých informací, které se předtím nikde neobjevily, a jejich práce je z technických i dalších hledisek zcela špičková, rozhodně ovšem nebyli první.
Takhle ne?
Práce nejspíš nebude v dohledné době vůbec žádný vliv na medicínskou praxi, a příliš zřejmě ani medicínský výzkum. Jde spíše o základní výzkum s neznámým potenciálem, navíc tak specifický, že se mu nejspíše bude věnovat nadále jen poměrně málo laboratoří.
Někteří odborníci dokonce označují celý experiment za v podstatě zbytečný, protože takto „editace genů“ rozhodně používat nemůže a nebude (viz například blog Noama Prywese a Jamese Kathe ). V případech podobných dědičných vad je totiž jednoznačně jednodušší a mnohem jistější nechat vyvíjet jen zdravá embrya - jak se samozřejmě ve značné míře dělá už dnes. „Editace“ jeho genů se zdá být jen náročný a drahý krok navíc.
Navíc je nutné dodat, že většina našich vlastností, včetně dispozic k nemocem, je ovlivněna stovkami či tisícovkami genů. My zatím zaprvé nevíme, zda náhodnou úpravou některých z nich nezpůsobíme nějaké problematické změny v jiných vlastnostech, za druhé neumíme geny upravovat ve velkém. CRISPR dnes může sloužit k úpravám maximálně desítek genů v jedné buňce, a to navíc za cenu výrazného zvýšení chybovosti.
Jistě se to může změnit. Právě CRISPR je hezký příklad toho, jak jeden nečekaný objev může vdechnout nový život celému odvětví a zamávat s odhady a předpovědmi - objevil se zcela nečekaně a otevřel úplně nové možnosti. Ale spíše než svůdně děsivému přemítání o budoucích nadlidech vytvořených na míru pro miliardářské dynastie, či masovému přepisování DNA druhu Homo sapiens (byť i to má v jisté míře smysl, samozřejmě) by bylo spíše záhodno věnovat se přízemnějším záležitostem. V první řadě vytváření rámce pro praktické využití této a dalších podobných technologií.
Peníze až v první řadě
Genové terapie, tedy hlavně již zmíněné „lokální“ úpravy genů některých tělních buněk v dospělém těle (třeba odstranění nějaké genetické oční vady), se zřejmě během několika let dostanou na trh. A zatím se zdá, že se bude opakovat nedávný scénář zavádění například tzv. biologických léků (tj. léků napodobujících látky vyskytující se v našem těle, například některé protilátky). To jsou léky někdy marginálně, ale často zásadně lepší než starší alternativy - protože jsou ovšem často extrémně drahé, jejich praktické nasazení nebývá úplně jednoduché.
Platí to i v České republice, jak ilustroval nedávný příklad muže s rakovinou ledvin, kterému pojišťovna jen velmi pomalu a vlastně až po medializaci případu schválila přechod na drahý biologický lék. Mimochodem s cenovkou zhruba 175 tisíc korun měsíčně.
První příklady genových terapií naznačují, že v případě genových terapií to může být podobné. Například první v Evropě dostupná genová terapie nazývaná Glybera na „opravu“ extrémně vzácné slinivky břišní letos stála pojišťovny něco přes 30 milionů korun na pacienta. Evropské úřady schválily její použití v roce 2012, ale samotný výrobce, holandská firma uniQure, si svolení nechá letos v říjnu vypršet: pacientů bylo málo, navíc se nevyplácí investovat do dlouhodobého sledování pacientů, které je podmínkou uvedení na trh.
Nápady, jak možný problém řešit, jsou různé. Jedním poměrně snadno představitelným je změna systému výplat pojištění - podle ní by pojišťovna za léčbu platila zpětně během následujících let (pokud by tedy pacient skutečně byl zdráv). Možná to samozřejmě nemusí být to správné řešení, ale debata o podobných „detailech“ je v tuto chvíli asi vhodnější než řešení hypotetických katastrofických scénářů. Mitalipov (a řada dalších) dokazují, že v budoucnosti by mohlo být možné leccos - ale rozhodně není jisté, že na to budeme mít.